
金属进行防腐目的在于避免腐蚀引起的外观变化或者内在功能的损失,自然界的大多数金属除了惰性金属比如金、银、铂等以单质形式存在,其他大多数金属都是以氧化物、卤化物、盐等形式存在,人们生产生活中常见的金属除了装饰品用到的贵重金属外,主要是铜、铜合金;铁、钢、不锈钢;铝、铝合金等,都是基于材料自身的电磁性能、力学性能而被应用。这些金属都有一个共同的特点就是俗称的生锈,此处有人会反驳不锈钢不生锈,这个问题后续会有解答。
首先弄清楚金属所生的锈是什么,锈是金属发生化学变化形成氧化物、硫化物、卤化物以及复杂盐类的概括性称呼,如铁锈是三氧化二铁和四氧化三铁,铜锈是绿色的碱式碳酸铜、铝锈是氧化铝和氢氧化铝等。锈变有如下几个特点:
①金属化学性质较为活跃,能够和自然界的常见物质如氧气、水、二氧化碳、硫化氢等接触后生锈,例如:按照化学活泼性从高到低的顺序依次有钾、钙、钠、镁、铝、锌、铁、锡、铅、铜、汞、银……
②从金属表面开始,向内部延伸,最具代表性的就是钢材的锈穿。
③发生金属锈变的其他条件如氧气、水汽、温度等
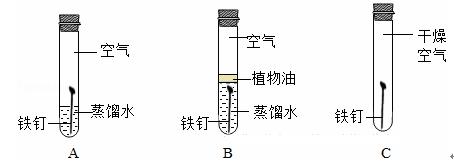
中学化学教材中有一个经典实验,用来探索金属腐蚀的一般特点,三个烧杯中各有一个铁钉,第一个烧杯中是空气,第二个烧杯中铁钉在水底、第三个烧杯中铁钉悬挂在水面,露出一半。一段时间过后发现第三个烧杯中的铁钉锈蚀最明显、水底的铁钉锈蚀最轻,这个现象充分证明了上述的第三个特点。
只有清楚了锈蚀的一般性规律和特点才能有针对性的采取防锈方法。科学技术的持续发展已经在金属防腐的多个方向上取得了显著成就,可以称之为“表面功夫”和内功都很优秀。下面就从内外两方面简单说明一下:
一、根据化学元素的特点进行混合实现由内而外的防腐,这个过程要符合实际、考虑经济适用性,所以出现了不锈钢、耐候钢而不是金铁合金;
二、做好表面功夫,既然生锈是由表及里,那么对表面进行一定的防护处理,阻断生锈的进行。这种思路最直接也最容易实现,采用物理或化学方法对外界有害介质进行隔绝从而实现防腐如浸油、涂覆凡士林,喷涂油漆,喷塑、静电喷涂、热喷涂、电泳、锌铬涂层、搪瓷、电镀铜铬涂层、烤蓝、磷化、阳极化处理、发黑处理等。这些表面工艺的共同特点是隔绝保护,除此之外还有牺牲保护,牺牲保护可以形象的理解成一道不够坚固的防线虽然不能抵御介质入侵,但是能够迟滞入侵过程,最具代表性的牺牲保护是镀锌(热浸镀锌,电镀锌、粉末渗锌),镀锌的厚度和致密性如同防线一样,越致密越厚则越能抵御腐蚀,防腐时间也就越长。

最后要回归开头提到的不锈钢的问题,不锈钢之所以“不锈”的本质是这类金属合金中铬含量达到一定的比例后(10.5%Wt),能在表面形成一层连续且致密的铬氧化膜(Cr2O3),因为其透明且具有自修复能力,所以金属表面始终能呈现金属光泽,即便局部Cr2O3被破坏也能快速修复再次封闭金属表面,但是即便如此也不是毫无缺点,这类氧化膜容易被卤化物破坏,所以海洋环境中使用的不锈钢有更加严格的成分要求。
本文链接:https://www.njmkt.net/Article/mktlgtjsff.html
(编辑者:南京曼卡特,如需转载,请注明出处)